Nátrium-foszfát
ortofoszfátok, pirofoszfátok (difoszfátok) és kondenzátumok. nátrium-foszfátok. Kristályos. vagy üveges anyagok, jól oldódóak. vízben kristályos hidrátokat képeznek (lásd az 1.2. táblázatot). A ortofoszfát Na3P04. A NaH2PO4 és a Na2HP04 fotofaktorok fotofrakciójának d és g-jeit kölcsönösen előállítottuk. H 3PO 4-et Na2C03-mal vagy NaOH-dal. a sók kikristályosodása és vízmentes sók vagy kristályos hidrátok NaH2P04. H2O, Na2HP04. 12H20 és Na3P04. 12H20. Ez utóbbit úgy is előállíthatjuk, hogy az AlPO 4-t Na2C03-mal 900 ° C-on melegítjük. vízzel való kimosódás és a p-ra kristályosítása.
A Na4P2O7 pirofoszfát polimorf; trihidro-NaH3P2O7. dihidro-Na 2 H 2 P 2 O 7 és gidropirofosfaty Na3 HP2 O7 felett bomlik 250 ° C-on, hogy egy kondenzált N. f. Készítette semlegesítése H 4P 2O 7, alkáli-kiszáradás dibázikus Na, Na3 HP2 O7 x x 9H 2 O-p-ra savanyítás Na4 P2 O7 sósavval az egyhez.
1. táblázat: A NÁTRIUM ORTHO- ÉS PYROFOSPHÁTOK TULAJDONSÁGAI
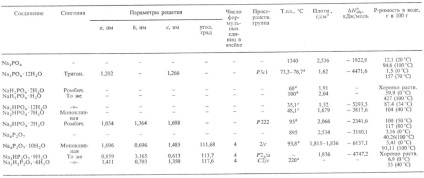
a Vízveszteséggel, teljes víztelenítés 100 ° C-on.> Teljesen kiszáradás 95 ° C-on. teljes elválasztásnál C> 5 vízmolekula elvesztése. q 1 molekula vizet veszít, nem olvad.
Táblázat. 2. KONDIDÁLT NÁTRIUMFOSFÁTOK JELLEMZŐI
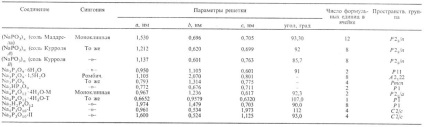
Hagyományos N. f. (elavult nátrium-metafoszfátok) tartalmaz egy csoportot (PO3) -. A polifoszfátok lineáris lánc szerkezetűek, ciklofoszfátot (NaP03) tartalmaznak. ahol n = 3,4,12-ciklusos.
A tetraciklopofoszfát Na4P4O12 lehet konformációs szék vagy kád. A vízmentes só csak a fürdő konformációjában ismert. A Na-tetraciklopofoszfátot az előállítási eljárással állítjuk elő. ekvimoláris mennyiségű NaH2P04 és H3P04 400 ° C-on az utóbbiakkal. az olvadék lassú hűtése. A kapott Na2H2P4O12-ot a NaOH képlettel semlegesítjük. Et al. az eljárás a H 4 P 4 O 12 oldat alkálifém pH-jának hűtéssel pH 7-re történő semlegesítésére szolgál.
Oligomer trifoszfát Na5P3O10. amely lineáris lánc szerkezettel rendelkezik, két változatban létezik, az m-átmenet II 417 ° C. A Graham sója és Na4P2O7 keverékének megolvasztása az utóbbiakkal történt. lassú hűtés, Na2HP04 és NaH2P04 elegyének dehidratálása 350-400 ° C-on (II. forma) vagy 500-550 ° C-on (I). A trifoszfát mennyisége az iparban gyártott összes 70% -a, lúgos foszfátok.
N. f. használt komponensek detergens -in, mint a víz lágyítószerek, detergensek, fémtisztítás, felületaktív anyag a pro-ve cementek és olajkút fúrása. Különösen jó detergens hatás szintetikus. Mosószerek nátrium-trifoszfát hozzáadásával (10-50%). A víz keménységének kiküszöbölése érdekében dehidratált NF-t használunk. komplexeket alkotnak Mg, Ca, Ba és más fémekkel. N. f. az ércek dúsításánál, foszfátüvegek, festékek, stb. előállításához adalékként vagy nyersanyagként, textilellenes segédanyagként használják. in-va, az élelmiszerekben. Prom-sti (kelesztő tésztát homogenizáljuk és konzisztenciájának javítására sajt, kolbász, sűrített tej), a fényképészetben (komponens fejlesztő) Elektrolitikus. folyamatok stb.
REFERENCIÁK Corbridge D. Foszfor. A kémia, a biokémia, a technológia, a transz. angolul. M. 1982; Átfogó szervetlen kémia, szerk. írta J.C. Bailar, A. F. Trot-man-Dickenson, v. 1, Oxf. 1973. L. Komissarova, P. Melnikov P.
Kémiai enciklopédia. - M. Soviet Encyclopedia. Ed. I. L. Knunyants. 1988.