Előadás az 1. előadáshoz
Az IUPAC szabályai az alkánok nevének megépítésekor az alábbi cselekvési sorozatot ajánlják.
1. Válassza ki a leghosszabb láncot, és nevezze meg az ősi struktúrát.
Ez a név lesz az alkán név gyökere.
2. Sorolja fel a szénatomokat úgy, hogy a molekula kezdetéhez legközelebb eső szubsztituens megkapja a legkisebb számot.
3. Sorolja fel a helyettesítőket ábécés sorrendben, jelezve minden lokant előtt, vagyis azon fő lánc szénatomjának a számát, amelyhez a szubsztituens kapcsolódik.
"Metán" nómenklatúra: az alkán metánszármazéknak tekintendő, amelyben egy vagy több hidrogénatomot szénhidrogéncsoportok helyettesítenek, például:
Metán nómenklatúra: tetra (terc-butil) -metán IUPAC elnevezési bonyolultabb: 2,2,4,4-tetrametil-3,3-di (terc-butil) -pentán
Egyes alkánok DH-elégése Energia kötések az alkánmolekulákban
KEY WORDS: alkánok, paraffinok, # 963; -bond, sp3 hibridizációs, izoméria szénvázat csoport, egy szabad gyökös mechanizmussal gyökös szubsztitúciós reakció, halogénezés, nitrálás, repedés, dehidrogénezés, izomerizáció, aromatizálást, dekarboxileződés, a Kolbe elektrolízis, Wurtz reakció.
AZ ALKANS HOMOLÓGIAI SOROK ÉS FIZIKAI TULAJDONSÁGAI
Az Alkanes egy nem ciklikus szerkezet végső szénhidrogénje. Paraffinoknak is nevezik őket.
Az alkánok homológ sorában az olvadási és forrási hőmérséklet az anyagok molekulatömegének növekedésével nő (1. táblázat). A metán, az etán, a propán és a bután - gázok színe és szaga nélkül. 5 - 15 szénatomszámú alkánok normál körülmények között, színtelen folyadékok, szénhidrogénből C16H34 - szilárd, fehér, viaszszerű anyagokból kiindulva.
Egyes normál alkánok képletei, nevei és fizikai tulajdonságai
Az Alkanes gyakorlatilag vízben oldhatatlan, de könnyen oldódnak nem poláros szerves oldószerekben, például benzolban. A folyékony alkánok sűrűsége valamivel kisebb, mint a vízé.
ALKANOV MOLEKULÁK SZERKEZETE
Az alkánmolekulák mindegyik szénatomja négy egyszerű # 963; -Changok hidrogénatomokkal vagy más szénatomokkal. A szénatomok elektronikus pályája a sp3-hibridizáció állapotában van. A hibrid orbitálok, és így az egyes szénatomok kötései a tetraéder csúcsai felé irányulnak (1. ábra).
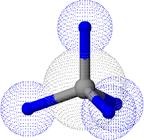
1. ábra Metánmolekulák modelljei: a - félgömb alakú; b - gömbkar (az elektronsűrűség megoszlása látható).
A metánmolekula és homológjainak valenciája 109,5 # 9702;. Ezért az alkánmolekulák szénláncának cikcakk alakja van:
körül # -C-S kötések, forgatás lehetséges, aminek következtében a molekulák különböző formákat vehetnek fel, úgynevezett konformációk (2. ábra).
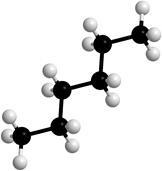
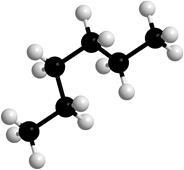
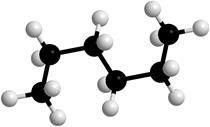
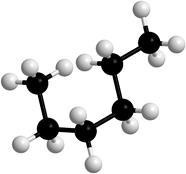
2. ábra: A hexán molekulák modelljei különböző konformációkban.
Az alkánmolekulák szénvázának normális lehet. és egy elágazó szerkezet. A metán homológ molekulákban az elsődleges molekulák megkülönböztethetők. másodlagos. tercier és kvaterner szénatomok (lásd az 1. függeléket).
Az alkánmolekulákban a C-C kötések kovalens nem polárisak, és a C-H kötések kovalens polárisak. Azonban a szén- és hidrogénatomok elektronegativitási értékei szorosak és egyenlőek 2,5-tel és 2,1-tel Pauling-szel. Ezért a C-H kötés tulajdonságai közel vannak a nem polárishoz, és hajlamosak homolitikus szakadásra a szabad gyökök képződésével:
Ennek következtében az alkánokat olyan reakciók jellemzik, amelyek egy radikális mechanizmus mentén haladnak.
Az IUPAC ajánlásaival összhangban a következő szabályokat kell figyelembe venni az alkánok megnevezésekor.
1. Keresse meg a fő, azaz a leghosszabb szénláncot. A fő lánc neve megegyezik az azonos számú szénatommal rendelkező alkán nevével (lásd 1. táblázat). A -an azt jelöli, hogy a szénhidrogén az alkánok osztályába tartozik.
2. Adjuk meg a fő láncban levő szénatomokat, a végétől az első rendelkezésre álló szubsztituenshez közelebb.
3. Formázza az alkán nevét. Erre a célra szubsztituensek listát alfabetikus sorrendben (például első etil- m, akkor E til-) mutató előtt mindegyik szubsztituens a szénatom száma a fő lánc van, amelyhez kapcsolódik, és adjuk hozzá a nevét a fő lánc.
Ha ugyanazok a szubsztituensek kettő, három vagy négy, akkor szorozzuk meg a di- előtagokat. tri- és tetra-.
Egy példa. Nevezzünk olyan alkánt, amelynek szerkezeti képletét alább mutatjuk be.
Az alkán formula leghosszabb szénláncát félkövéren mutatjuk be. 8 szénatomot tartalmaz. Az azonos számú szénatommal rendelkező alkánt oktánnak nevezik. Ez a szó fog alapul venni az egész anyag nevéhez.
Három szubsztituens van a molekulában - két CH 3 csoport és egy CH 3 -CH 2 -. Ebben az esetben a szénatomok számozása jobbról balra, akkor a szénatom, amelyhez a lánc kezdetéhez legközelebb eső CH3-szubsztituens kapcsolódik - a 2. számú lesz.
A helyettesítőket alfabetikus sorrendben soroljuk fel, jelezve minden egyes számjegyhez annak a fő láncnak a szénatomszámát, amelyhez csatoltuk, és adjuk hozzá a fő lánc nevét # 8209; az oktán szó.
Tehát az alkán neve 2,6-dimetil-3-etil-oktán.
Az alkánok esetében csak egyfajta szerkezeti izomerizmus létezik # 8209; a szénváz izomerizmusa.
Az alábbiakban találhatók a C6 H14 hexán összes izomerjének szerkezeti képletei.
Az IUPAC szabályai az alkánok nevének megépítésekor az alábbi cselekvési sorozatot ajánlják.
1. Válassza ki a leghosszabb láncot, és nevezze meg az ősi struktúrát. Ez a név lesz az alkán név gyökere.
2. Sorolja fel a szénatomokat úgy, hogy a molekula kezdetéhez legközelebb eső szubsztituens megkapja a legkisebb számot.
3. Sorolja fel a helyettesítőket ábécés sorrendben, jelezve minden lokant előtt, vagyis azon fő lánc szénatomjának a számát, amelyhez a szubsztituens kapcsolódik.
"Metán" nómenklatúra: az alkán metánszármazéknak tekintendő, amelyben egy vagy több hidrogénatomot szénhidrogéncsoportok helyettesítenek, például:
Metán nómenklatúra: tetra (terc-butil) -metán IUPAC elnevezési bonyolultabb: 2,2,4,4-tetrametil-3,3-di (terc-butil) -pentán
Egyes alkánok DH-elégése Energia kötések az alkánmolekulákban