nitrálásával klór-benzol

Home | Rólunk | visszacsatolás
Klóratom, mint ismeretes, van egy negatív induktív hatás vagy pozitív mezomer hatása, -I-hatású -effect meghaladja a + M. Így, az elektron akceptor jelentése klóratom és akadályozza az áramlást a elektrofil szubsztitúciós reakciók. Ezért, a nitrálási klórbenzol bekövetkezik 7-8 szer lassabb, mint a nitrálási benzol. Mindazonáltal, a reakció sebessége elegendően nagy, és a folyamat szervezett folyamatos módon egy kaszkád három vagy négy reaktor. Kezdjük nitrálást 20-40 ° C-on (első reaktor), és a végén - 70-80 ° C-on (az utolsó reaktor). Az utolsó reaktorból, a reakcióelegy belép a fázis elválasztó, ahol az elválasztás a hulladék savat (alsó réteg) a szerves réteget (felső réteget). Nitrochlorobenzene elegyet egymást követően mossuk vízzel, szóda oldattal és ismét vízzel mossuk, vákuumban szárítjuk, és ezután irányítják a szétválasztás, amelynek alapja a kémiai tulajdonságai eltérnek mononitrohlorbenzolov.
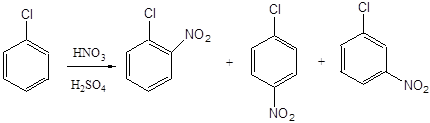
körülbelül 30%, körülbelül 70% és 1,5%
A gyakorlati jelentősége a három izomer nitrochlorobenzene vannak para- és orto-izomerek, amelyekben a klóratom pedig aktív pozícióban, és egy nitrocsoportot könnyen helyettesíthető különböző kategóriákba eredményeként a nukleofil reakciókat. Így a p-nitrochlorobenzene nyerhető p-nitro-fenol, p-nitrofenetol, p-nitro-anizolt, p-nitro-anilin, difenil-amin, és a különböző származékai difenil-éter. A nitro-csoportot a fenti vegyületek (kivéve a p-nitro-anilin) et azt követően csökken az amino-csoport. A következő rendszereket lehet javasolt példaként:
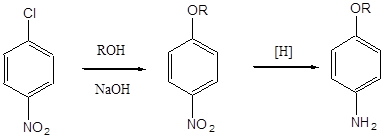
R = H p-nitro-fenol, p-amino-fenol
R = OCH3 p-anizidin p-nitro-anizolt
R = OC 2H 5, n-p-fenetidin nitrofenetol
klóratom, a 2,4-dinitro is könnyen esetben különböző csoportok eredményeként a nukleofil reakciókat. Különösen, az intézkedés alapján vizes alkáli-oldatot (nátrium-hidroxid), vagy ammóniával ad 2,4-dinitro-fenol és 2,4-dinitro-anilin. Mivel az egyik technológiák 2,4-dinitro-fenol így kapott nitrálást nyerhető pikrinsav.
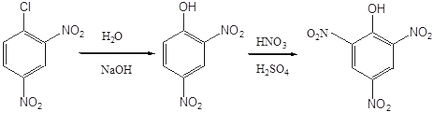
Pikrinsav. MP 122-122,5 C. felrobban upon detonációs érintkezve fémek és oxidok előállításához felhasznált azoszínezékek, magas robbanóanyagok, azonosítására különböző szerves vegyületek. Ez egy erős sav, amely összehasonlítható az ásványi savakkal. pikrinsav sójává említett pikrátok. Egy pikrátok bocsátanak ki különböző illékony szerves bázikus vegyületet.
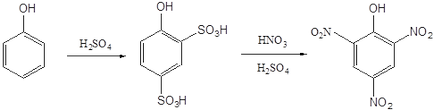
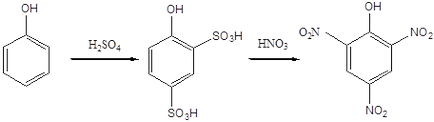
Hasonlóképpen, 1-naftol, 1-hidroxi-2,4-dinitronafta-lin.
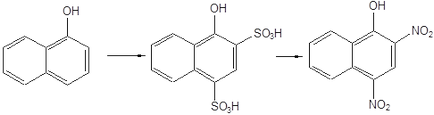
Az amino-csoport még erősebb elektrondonor szubsztituenst, mint a hidroxi-csoport. Ugyanakkor az aminocsoport könnyen oxidálódik. Ezért a közvetlen nitrálást aromás aminok lehetetlen. Ebben a tekintetben, amino-védő korábban. Általában védelmére használt acetil- vagy tozilcsoport. A atsilnyh- N-tozil- vagy N-származékai aromás aminok a bázikussága aminocsoportot egy érzékelhető mértékben csökken. Nitrálása ezen vegyületek végbemegy túlnyomórészt para-helyzetben védett aminocsoport. A védőcsoport a nitrogén-termékeket ezt követően eltávolítható eredményeként bázikus vagy savas hidrolízissel. Példaként képviseli a rendszer előállítására 2-metoxi-4-nitro-anilin.