Egy lecke a "hidrogén felfedezés történetéről"
másolat
1 Városi költségvetési általános oktatási intézmény "Gredyakinskaya általános általános iskolai oktatás" Tanulmány a téma: "A történelem a felfedezés a hidrogén. A hidrogéntermelés módszerei a laboratóriumban és az iparban »
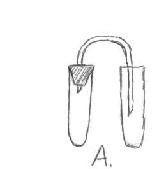
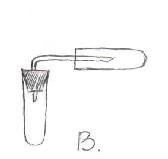
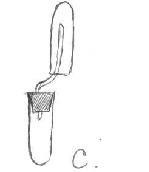
3 - Eszköz Kippa eszköz (megmondja és bemutatja a tanárt) 2) A savas oldat hatása a fémekre. A kísérlet bemutatása: A reakció hasonló a víz forrázásához, a cink a hidrogénatomokat helyettesíti, a cinkklorid sót a szubsztitúciós reakció eredményeként alakítják ki. Zn + 2HCI ZnCI 2 + H 2 Zn + H 2SO 4, ZnSO 4 + H 2 egyszerűsége miatt a hidrogén által gyűjtött az elmozdulás a levegő és a víz, lenyomva tartja a cső nyílása. 3) Az aktív fémek kölcsönhatása vízzel. Általában ezek a reakciók hevesen zajlanak, ezért egy kis fémdarabot kell venni. Egy hidrogénatomot elválasztunk a vízből, és OH egy vegyértékű hidroxilcsoport képződik, a fématom hozzákötődik ahhoz, hogy egy bázist vagy hidroxidot képezzen. 2Na + 2HOH 2NaOH + H 2 Sh. Hidrogéntermelés az iparban. 1. Általánosságban a földgázból átalakítással (átalakítással) kapott vízgőz és katalizátor hatására. CH 4 + 2H 2 O Ni 4 H 2 + CO 2 gőz 2. Fűtés. CH 4 Ni 2H 2 + C 3. A víz áramlás hatásának bomlása. 2H2OH2 + O2 IV. Az alábbi eszközök közül melyik használható hidrogén előállítására? Kérdés: Milyen okok alapján állapíthatja meg a hidrogén jelenlétét a kémcsőben? V. Laboratóriumi tapasztalat. "A hidrogén megszerzése és tulajdonságai" (a notebookban rögzítve) 1. Biztonsági technológia. - Óvatosan dolgozzon az asztalon, - Ne engedje, hogy a savak belépjenek a bőrbe és a ruházatba. - De ha mégis savanyúvá teszed a bõrét, törölje le egy rongyot és mossa meg a kezét. 2. Hogyan fogjuk és gyűjtünk hidrogént? a) Először 5 darab cinket helyezzünk a kémcsőbe, és adjunk hozzá 5 ml sósavoldatot. b) Zárja le a csövet parafával egy gázcsővel, c) Gyűjtse össze a hidrogént egy üres tiszta kémcsőbe, és tartsa a csövet lyukkal lefelé. 3. Hogyan igazolható a hidrogén jelenléte a kémcsőben? (Ez azért fontos, hogy a cső a hidrogén láng, és ha összegyűjtjük tiszta hidrogén, hallod gyapot „n ágyék”, ha a hidrogén levegővel összekeverve, a ugatás pamut hallható).
ha ($ ez-> show_pages_images $ page_num doc ['images_node_id'])
4 4. A munka teljesítménye: Feladat: a). Mit figyeltél meg, amikor a kémcsövet hidrogénnel hozta a lánghoz? (vízcseppek a kémcső falán) b). Milyen anyagok képződnek a hidrogén égéséből? (Víz és hőt termel) Record reakcióegyenlet H2 O2 + 2H2O Következtetés: Megtanultuk, hidrogén és hogy ellenőrizze annak jelenlétét, hidrogént vezetünk be a kémiai tulajdonságokkal jelentése hidrogénatom égő oxigénből víz képződik. VI. Biztosítása 1.Zadanie- rejtély (a táblára írt levelek, meg az üzenetet a tudós) Minden kísérletet félretett számítások vannak szakítva reggel utazás sokkal tudósok fog hirtelen kalap dobni a sarokban! Az asztalhoz rohan! Rettenetes hangon van, és nem hall valamit: "Ne felejtsd el figyelmeztetni, hogy megakadályozz egy szörnyű robbanást". Mit írtak a tudós a kollégáinak ebben az üzenetben? S C D OD A C C S "Hidrogén és oxigén keveréke M E V O R O D O R O L vagy levegő robbanásveszélyes." 2. FEJEZET: Három, gázzal töltött cső Egy levegőben; a másikban a hidrogén; a harmadik oxigénben. Honnan tudja, melyik kémcső mely gáz? 3. Adjunk hozzá sósavat (HCl) a kémcsőbe vasfűrészrel Írjuk le a Fe + 2HCI- = FeCl2 + H2 reakcióegyenletet. 4. Kémiai diktálás. Soronként 8 sor. Minden számra írja le a gázképletet. Н 2 1. Világos gáz О 2 2. Nehézgáz О 2 3. Gáz, támogató égés Н 2 4. A gáz oxigénnel keveredik és normál körülmények között felrobban. H 2, O 2. 5. Szerelje össze a levegő elmozdulását. H Az edényt gyűjtsük össze az O 2, H 2 tartályban. 7. Gyűjtsük össze a víz eltolásával. 8. Gyűjtsön össze egy aljába helyezett edényben. Kb.